欢迎来到领伯医汇(杭州)医疗科技有限责任公司官网!
联系电话:0571-86110687

请输入网站标题
清空记录
历史记录
取消
清空记录
历史记录

搜索
取消
清空记录
历史记录
清空记录
历史记录
医疗器械创新申报
2014年2月7日,原国家食药监总局发布了《创新医疗器械特别审批程序(试行)》,自2014年3月1日起施行,该程序是在确保上市产品安全、有效的前提下,针对创新医疗器械设置的审批通道。
产品详情
医疗器械创新申报
2014年2月7日,原国家食药监总局发布了《创新医疗器械特别审批程序 (试行)》自2014年3月1日起施行,该程序是在确保上市产品安全、有效的前提下,针对创新医疗器械设置的审批通道。2018年11月,国家药监局发布《创新医疗器械特别审查程序》,境内、境外申请人均可按照该程序要求,提交相应技术资料及证明性文件,提出创新医疗器械特别审查申请。
产品创新性初步界定 创新申报可行性评估 创新申报文件流程办理及材料指导
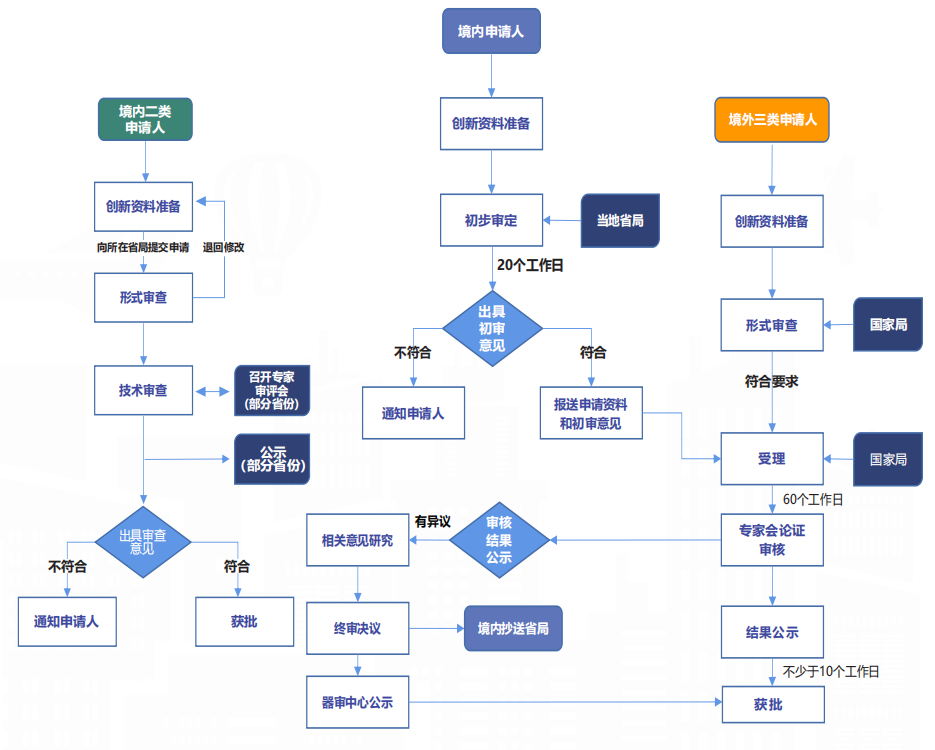

医疗器械创新申报
2014年2月7日,原国家食药监总局发布了《创新医疗器械特别审批程序(试行)》,自2014年3月1日起施行,该程序是在确保上市产品安全、有效的前提下,针对创新医疗器械设置的审批通道。
产品详情
医疗器械创新申报
2014年2月7日,原国家食药监总局发布了《创新医疗器械特别审批程序 (试行)》自2014年3月1日起施行,该程序是在确保上市产品安全、有效的前提下,针对创新医疗器械设置的审批通道。2018年11月,国家药监局发布《创新医疗器械特别审查程序》,境内、境外申请人均可按照该程序要求,提交相应技术资料及证明性文件,提出创新医疗器械特别审查申请。
产品创新性初步界定 创新申报可行性评估 创新申报文件流程办理及材料指导

相关业务

选择区号
 浏览器自带分享功能也很好用哦~
浏览器自带分享功能也很好用哦~





