欢迎来到领伯医汇(杭州)医疗科技有限责任公司官网!
联系电话:0571-86110687

请输入网站标题
清空记录
历史记录
取消
清空记录
历史记录

搜索
取消
清空记录
历史记录
清空记录
历史记录
原创:血氧类产品临床准确度评估
在我国,医疗器械按照风险程度,共分为三个管理类别,血氧类产品风险程度适中,被界定为第II类医疗器械,其分类代码为:07医用诊察和监护器械,主要包括脉搏血氧仪、血氧传感器、指夹式血氧仪。 部分有创多参数监护仪中含有血氧模块,其类别为第III类。
2022-12-28 11:14:06领伯医汇(杭州)医疗科技有限责任公司
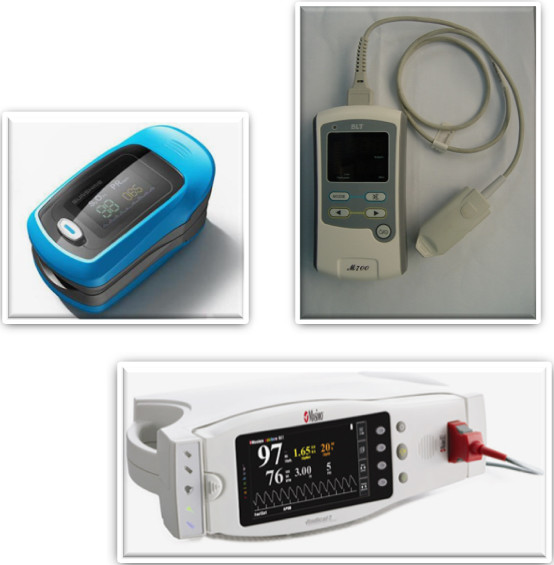
第II类医疗器械,需要获得省级药监部门的批准,获得第II类医疗器械注册证,才能够上市销售。
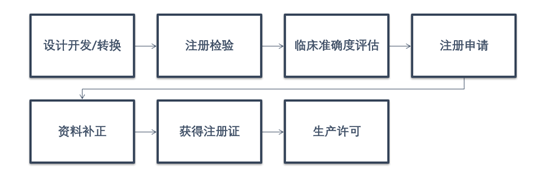

临床评价
准确度评估
Q:申报单位是否需要按照临床试验程序,进行准确度验证?
A:产品虽然已经豁免临床试验,但是临床准确度人体评估,需要经过临床确认。该类验证考虑到需要进行动脉穿刺、降低吸入氧浓度、动脉置管与抽血,故在操作上,对受试者有潜在的风险。对于此类产品,应该在临床医院开展,且需要经过伦理委员会的批准。认为在实验室(非医疗机构)的验证,不具备保护受试者的硬件条件,且无相关的伦理学程序。其数据、结果的可信度不高。
Q:若进行无创法研究,应如何进行?
A:若选择无创法进行对比,受试者无需进行抽血,对比器械应进行过有创的临床试验。需要获取对照器械的SaO2数据。
Q:对于探头的准确度评估,是否可以只做一个代表型号?
A:对于企业申报的探头种类较多时,可以只对代表型号进行准确度评估。企业应根据探头的结构组成、光电元器件、适用人群、与人体的贴合方式、适用部位,确定代表型号。
Q:如何联系你们?
A:您好,可以点击上方蓝色字即可关注我们!或了解更多咨讯可以扫描下方二维码或电话联系我们的商务经理。

相关新闻

选择区号
 浏览器自带分享功能也很好用哦~
浏览器自带分享功能也很好用哦~